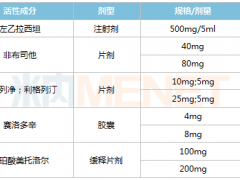
左乙拉西坦注射液是由UCB研发的一款抗癫痫药,最早于2006年在美国上市,2021年优时比的左乙拉西坦全球销售额达9.7亿欧元(以4月1日汇率计,约10.7亿美元)。目前在美国境内,左乙拉西坦注射液的主要生产厂商包括Viatris、Aurobindo、Hikma等。
而在国内市场,华海药业于2020年11月以仿制4类提交左乙拉西坦注射用浓溶液上市申请,近日已步入行政审批阶段,有望于近期获批。
非布司他片是由Tekeda研发的一款黄嘌呤氧化酶抑制剂,主要用于痛风患者高尿酸血症的长期治疗。原研产品最早于2009年3月在美国上市,目前在美国境内,非布司他片的主要生产厂商有Viatris、Sun、Alembic等。
华海药业的非布司他片ANDA于2018年5月获得FDA暂时批准,此次为正式获得批准。而在国内市场,华海药业曾于2014年提交非布司他片上市申请,之后主动撤回,目前还处于开展BE试验阶段。
华海药业表示,左乙拉西坦注射液ANDA文号的获批及非布司他片获得正式批准,标志着公司具备了在美国市场销售上述产品的资格,这有利于公司不断扩大美国市场销售,强化产品供应链,丰富产品梯队,提升公司产品的市场竞争力,对公司的经营业绩产生积极的影响。
2022年至今华海药业获批的ANDA
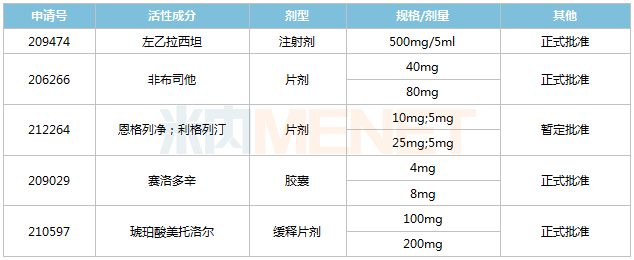
来源:米内网全球上市药物库
米内网数据显示,含左乙拉西坦、非布司他在内,今年以来华海药业已有5个ANDA获得FDA批准,其中恩格列净利格列汀为暂定批准。
来源:米内网数据库、上市公司公告等
注:数据统计截至4月1日,如有疏漏,欢迎指正!